纳米药物递送体系有多种类型和功能,本文将简介纳米递送药物体系介导氧化还原反应物质的递送,应用于氧气的靶向输送。
1. 纳米药物递送体系
近几十年来,纳米技术的快速发展使得多种生物医学应用的纳米平台被设计构建用于疾病的诊断治疗。用作药物递送系统的纳米颗粒一般是亚微米级颗粒(3-200nm),纳米系统种类繁多,可以使用各种有机及无机材料进行构建,包括但不限于聚合物(如聚合物纳米粒子,胶束或树枝状聚合物),脂质(脂质体),蛋白质(白蛋白,转铁蛋白),病毒(病毒纳米粒子),有机金属化合物(纳米管,MOF),甚至细胞衍生的纳米粒(如红细胞、肿瘤细胞、干细胞)。纳米载体作为药物递送系统具有其独特优势:首先是它的粒径优势,纳米级的粒径使其具有较大的比表面积,因此,纳米系统通常具有很高的载药量;其次由于纳米粒表面可以修饰配体达到靶向特定组织器官的作用,如修饰了叶酸分子的纳米粒可以有效靶向肿瘤组织、缀合去铁铁蛋白的纳米粒具备肾脏蓄积能力等,从而控制系统在指定的时间地点释放药物,达到精准治疗的效果;除此之外,纳米粒还具有疏水药物增溶、延长药物体内半衰期等独特的作用,在生物医学应用中有着不可复制的优势
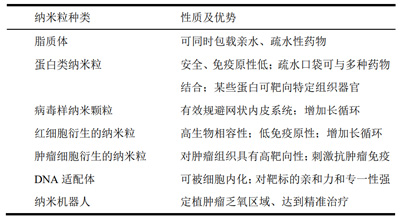
表 1.不同种类的纳米递送系统及各自的优势
2. 基于全氟化合物的纳米氧载体
一直以来,都有许多研究致力于开发不同种类的纳米氧载体,如血红蛋白类氧载体、全氟化合物类氧载体等,以期使用纳米技术达到递送氧气、逆转组织乏氧的效果。相比较之下,血红蛋白类氧载体有两点弊端:①游离的血红蛋白中含有血红素分子,会对机体造成不可逆转的肾脏损伤、自氧化损伤;②血红蛋白与氧分子是可逆化学结合,导致其不能向周围组织释放全部溶解的氧气,而全氟化碳与氧气则是单纯的物理溶解,有研究表明,溶氧量相同时,血红蛋白的释氧量仅为全氟化碳的26%。因此,基于全氟化合物的纳米氧载体由于其优越的载氧释氧能力、较高的组织相容性和安全性成为其中较具临床潜力的一类纳米递氧系统。
全氟化碳是一种氢原子全部或部分被氟原子取代的烃类物质,它的化学惰性很强、组织相容性较好。全氟化碳的溶氧量大约在40-50vol%,在相同氧分压下,它的载氧能力大约是水和血浆的20-25倍,这种高载氧能力使其在临床研究中被开发用于血液替代品、肿瘤氧合以及器官保存灌注液。早在上世纪90年代,Fluosol®作为初代血液替代品进入临床,但由于其乳化剂泊洛沙姆F-68并不能很好地包裹全氟萘烷和全氟三丙胺,导致载药量偏低、临床递氧效果并不是很好,Fluosol®较终退出了市场。随后有研究全氟化合物乳剂的配方进行了改良,使用人血清白蛋白作为PFC载体,利用白蛋白的疏水空腔对同样具有高疏水性的全氟化碳进行包裹,极大地提高了纳米系统的递氧效率。
直到现在仍然有许多研究致力于全氟化合物在血液替代品中的应用。Zhang的课题组设计了一种用于体内氧输送的全氟化碳纳米乳。采用红细胞膜直接与全氟溴辛烷声乳化的方法制备纳米乳,得到的RBC-PFCs具有比全血更优越的载氧能力(图1c),并且RBC-PFCs能作为一种血液替代品在大鼠缺血性休克模型中迅速将平均动脉压(MAP)恢复至初始水平(图1d)
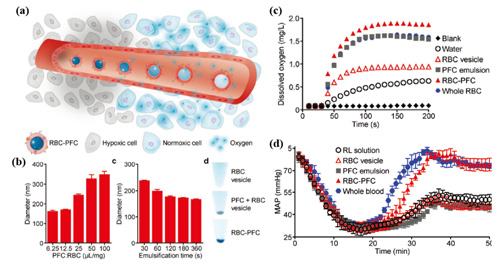
图1.PFC红细胞膜纳米乳作为血液替代品逆转大鼠缺血性休克
全氟化碳用于提高肿瘤氧分压、逆转肿瘤乏氧的研究也十分多见。Liu等人制备了一种中空PEG-Bi2Se3纳米颗粒,在其中负载了预饱和氧气的PFC液滴用于肿瘤氧合及放射增敏。在NIR光的照射下,氧气从PFC中大量释放,改变肿瘤内部乏氧环境并协同放疗增敏剂Bi2Se3增效放疗。类似地,Liu的课题组还设计了一种红细胞膜包裹的PFC@PLGA纳米粒,PFC的高携氧能力使其到达肿瘤后持续地为肿瘤供氧并同时增效放疗。吴锦慧教授课题组也在此前报道了一种红细胞膜包裹的珠蛋白全氟萘烷纳米乳剂,具有高载氧性质的全氟萘烷纳米乳剂能够在体内外达到长效供氧的效果并能够逆转乏氧导致的肿瘤放疗抵抗。

图2.PFC纳米递氧系统用于肿瘤放疗增敏
除此之外,基于全氟化碳的纳米氧载体也在器官移植中有着广泛的研究。如前所述的肾脏离体动态灌注保存方法,其中用于改善肾脏微循环的较常用的灌注液之一就是全氟化碳纳米乳剂。早在上世纪60年代,就有研究使用Fluosol-43全氟三丁胺纳米乳剂进行犬肾体外灌注保存,成功将肾脏离体保存20小时。作为肾脏保存的灌注液,全氟化碳乳剂有着不可复制的优势,首先全氟化碳的高载氧能力为肾脏组织提供氧气,从而保证正常有氧代谢维持细胞生理功能;其次全氟化碳具备溶解二氧化碳的能力,可以将组织细胞有氧呼吸产生的二氧化碳和代谢产生的废物带走。除此之外,在静态器官保存方法中,还有一种“两层法(”TLM)也是利用全氟化碳的高载氧能力向组织供氧(图3)。两层法是由神户大学研究人员发明,起初用于移植胰腺的保存,在此方法中,将PFC溶液与UW器官保存液(或Collins液)置于同一装置中,由于PFC的强疏水性会与器官保存液分成两层,这允许胰腺漂浮在两层溶液的界面之间,使得离体器官既能保存在器官保存液中,又能接受PFC供给的氧气,极大地提升了离体静态保存的效果。

图3. 基于 PFC 的“两层法”器官保存装置
3 基于二氧化锰的过氧化氢响应性纳米产氧体系
如前所述,在器官移植的缺血过程中肾脏组织高表达过氧化氢,同时,由于细胞的代谢方式的改变使得乳酸堆积,缺血损伤的肾脏pH值较低。不仅仅是器官移植,许多病理条件下都会引起过氧化氢的过表达。研究表明肿瘤微环境的过氧化氢浓度也异常增高,而且肿瘤细胞为了满足自身快速增殖的能量需求会上调无氧呼吸、增加糖酵解,这就导致乳酸的升高同样也会导致实体瘤部位较低的pH值。因此,基于二氧化锰的纳米氧气发生器引起了人们的研究兴趣,二氧化锰可与过氧化氢反应产生氧气,既能将组织不需要的过量H2O2清除,又能反应产氧,改善组织乏氧情况。反应过程如下:
MnO2+2H+=Mn2++H2O+1/2O2↑
MnO2+H2O2+2H+=Mn2++2H2O+O2↑
近年来,以此反应为基础设计了许多基于二氧化锰的过氧化氢智能响应纳米系统。Liu的课题组设计了一种pH响应的智能白蛋白-MnO2纳米系统。在这项工作中,人血清白蛋白被预先修饰上光敏剂二氢卟吩e6(Ce6)或顺铂前药(cis‐Pt(IV)SA),用于肿瘤化疗与光动力治疗的组合疗法。接下来,在碱性条件下,HSA能够进行生物矿化螯合Mn2+形成蛋白包覆的MnO2纳米团簇(HMCP)。响应于肿瘤微环境的酸性和丰富的H2O2,在一方面,HMCP能够在实体瘤内消耗过氧化氢原位产生氧气增强乏氧限制的PDT疗效;另一方面,HMCP能够降解为小尺寸的HSA-Ce6和HSA-Pt(IV)复合物,增强肿瘤渗透性从而显示出改善的光动力和化疗疗效(图4a)。在第二项工作中,Liu和他的同事利用阳离子聚合物PAH稳定MnO2纳米粒,并与光敏剂Ce6共轭,然后包覆聚丙烯酸PAA,交联聚乙二醇来增加整个纳米体系的稳定性和水溶性。结果显示,MnO2纳米粒能够逆转乏氧、增效光动力治疗

图4.过氧化氢响应性二氧化锰供氧纳米粒的构建
以上研究表明,在过氧化氢存在的环境下,MnO2纳米体系能够有效与其反应产生氧气,消耗过氧化氢、改善组织乏氧。然而遗憾的是,过氧化氢响应性MnO2纳米系统在肿瘤治疗中的研究比较多,而在与肿瘤具有相似病理环境(乏氧、过氧化氢增多、pH降低)的肾脏移植缺血损伤中还未见较多应用。因此,也可以预见纳米载药递送系统运输氧气的设计可为智能H2O2响应性纳米递氧系统在肾脏移植中氧自供从而免受缺血损伤打开了新思路。