脂质体是由双亲性的磷脂双分子构成的球体,如下图所示,脂质体内部可以包裹亲水性的药物,双分子层间可以包裹疏水性药物,结合脂质体具有:靶向性、缓释性、细胞亲和、组织相融、高生物安全性等特点,脂质体作为药物递送系统越来越受到重视。
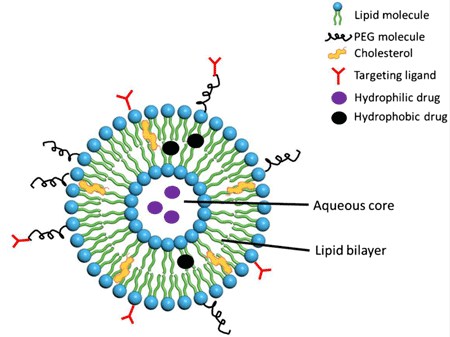
图 脂质体结构、修饰与包封示意图
根据一篇2017年FDA的统计文献记载,过500份脂质体药物递交了申请,其中约100份是作为联合疗法(与其他药物联合使用的脂质体药物)。其余的提交(脂质体单独使用)分别为3%NDAs,1%ANDAs和96%IND,包括Bio-INDs。
脂质体药物给药途径
统计的脂质体药物产品申请中,给药途径主要是静脉注射,占比84%。这是由于静脉给药途径是可使药物直接进入全身血液循环中,并具有100%生物利用度的较快方式。吸入是第二常见的给药途径,但目前还没有产品上市。针对吸入给药途径产品的大量开发的一个原因可能是由于通过吸入可以更有效地治疗一些疾病,例如哮喘、肺部感染、肺移植免疫抑制和肺癌等。吸入给药途径制剂的开发通常是复杂的,因为除了与产品处方相关的复杂性之外,传递装置的性质也成为质量控制的重要因素。此外,控制粒径分布和游离药物的百分比,在吸入性脂质体产品早期开发研究中是十分重要的。
脂质体产品适应症
递交的脂质体药物用于肿瘤(包括头颈部,肝,肺,血液)治疗占比可高达约63%。这是由于脂质体产品可以靶向于肿瘤位置而用于治疗多种类型的肿瘤。此外,抗肿瘤药物还存在溶解性和毒性问题,因此采用脂质体这种载体来传递药物是非常适用的。其他常见的适应症是感染(肺,真菌),眼部疾病和疼痛。
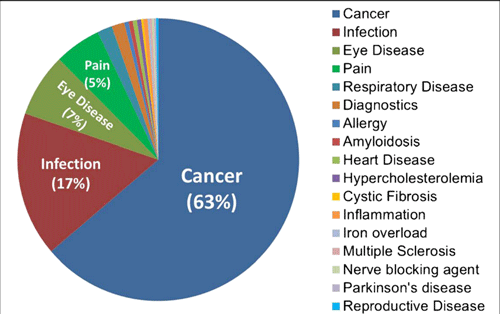
图 脂质体药物适应症统计
FDA审查脂质体产品中发现的质量问题统计和分析
FDA审查脂质体产品中发现的质量问题分为脂质体剂型特异性、非特异性2类。
脂质体剂型特异性问题如:脂质降解产物、脂肪酸组成、粒径、药物包封率、脂双层和脂质相转变温度等。因为这些参数是脂质体剂型的关键质量属性。类似地,在生产中涉及脂质体制剂的具体过程控制或生产细节也被认为是脂质体特异性的。特别是粒径和粒径分布是脂质体特异性质量问题,因为它影响着脂质体特异性CQAs。而使用Genizer微射流高压均质机以及脂质体挤出器制备的脂质体,可轻松实现粒径均一且满足认证要求。
1. 脂质体剂型特异性存在的问题
根据递交的材料显示,存在质量问题的产品中约47%为脂质体剂型特异性问题,详细描述如下;
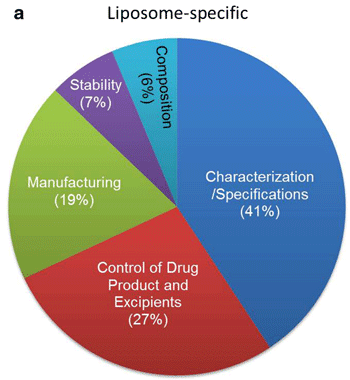
图 脂质体药物剂型特异问题
(1)产品性质与表征(41%)
由于脂质体自身具有复杂的物理化学性质,而且这些复杂的性质对产品的性能具有较大的影响,另外从产品批次间重现性,批次间释放相似性,以及在ANDAs的情况下比较仿制产品与参比药物(RLD)的角度来看,对脂质体产品(或原研产品)进行彻底的表征是十分重要的。表征的内容主要包括脂质体的CQAs,例如粒径大小,脂质体杂质,体外药物释放,脂双层,游离和包封药物比例等。这些CQAs中的一些项目是在监管机构审评提交的脂质体申报材料中常见的问题,详细讨论如下:
①粒径
脂质体的粒径和粒径分布影响着产品的体内生物分布和药物药代动力学等性质。为了达到仿制产品和RLD的一致性,平均粒径和粒径分布通常应处于相似的范围内。但用于报告的粒径参数可能会根据所使用的技术和仪器参数而有所不同。例如,用于测定粒径和粒径分布的常用技术手段是动态光散射(DLS)。但DLS的结果可能会根据仪器内置的算法和加权参数(强度,体积或数量)而变化。基于这个问题,在2015年发布了脂质体草案指南的修订版,指南已经将平均粒径的报告参数指定为体积或质量分布(如果粒子密度已知)。此外,脂质体产品的生物等效性(BE)指导原则建议将粒径的报告参数修订为具有多分散性的平均粒径(体积或质量分布);粒径分布(D10,D50和D90水平或具有SPAN的D50,即[(D90-D10) /D50])。FDA在进行审查时会具体问题具体分析,会根据每个产品根据自身的优点进行审查。因此FDA对于诸如粒径分布这样的项目没有给出全面的建议,而是由药品申请者提出,随后由FDA进行审查。
②脂质降解产物
一般情况下,很难完全确定脂质体产品的降解特征,特别容易忽视在产品生产和/或储存期间可能形成的溶血脂质。溶血脂质会导致相关的毒性问题(溶血和/或凋亡),因此对于溶血脂质含量的监测和控制属于关键质量参数,通常需要在生产过程和货架期期间监测和控制脂质体产品溶血脂质含量。
③体外释放
脂质体产品的体外释放试验可以用于了解产品的体内行为,并且还可以用于评估产品质量,生产过程控制以及CMC变化对产品质量的影响。另外体外释放方法还能够区分产品的可接受和不可接受的批次。2015年脂质体指南草案中鼓励建立脂质体产品的体外和体内相关性(IVIVC)或体外/体内关系(IVIVR),以建立合适的体外释放方法,来预测脂质体产品的体内性能。
(2)原辅料的控制(27%)
脂质辅料是脂质体生产的关键原料,并影响着脂质体产品的质量和性能。因此FDA在审查时要求提供有关脂质辅料的详细信息,其重要地位与原料药相当。脂质辅料的技术参数可以包括但不限于来源,理化特性和降解产物(特别是溶血磷脂)。通常基于ICH Q3B指南中确定的鉴定和定量阈值对脂质体产品中溶血磷脂和杂质/降解产物在进行监测和控制。此外,如果脂质辅料来源于动物组织,则应提供传染性或牛海绵状脑病(TSE / BSE)声明,进而对潜在的神经系统疾病风险进行适当的控制。
鉴于脂质体制剂的复杂性,应使用合适的分析方法来表征脂质体药物产品的CQAs,但这有时往往是困难的。使用不当的方法可能会产生错误的结果,从而使数据的可靠性被质疑,因此应提供分析方法的详细细节以及验证报告,以证明该方法是敏感、准确、、可靠和稳定的。没有这些方法的细节和验证数据可能会对用于评估质量属性的分析方法的准确性和可重复性的产生担忧。用于表征CQAs不适当方法的实例是使用测定粒径常用的动态光散射(DLS)方法来测定游离和包封的药物比率;使用相对不灵敏的薄层色谱法来测定未知杂质;使用不能区分可接受和不可接受产品批次的体外释放方法。
(3)生产(19%)
药物申请将要提供有关生产步骤,使用设备,完整流程图(包括起始原料,生产步骤和过程控制(IPC))以及持续时间(如适用)的完整信息。脂质体的生产是一个复杂的过程,每个生产步骤都应通过适当的IPC进行仔细控制和监控,以获得产品良好的重现性。
FDA在审查脂质体过程控制资料中确定的挑战方面如下:
①应在减小粒径的步骤前后分别测定粒径和粒径分布,以监测所采用粒径减小技术的有效性。
②应确定过滤器/膜完整性,挤出后的单个脂质组成变化,渗滤和无菌过滤以监测过滤/挤出的有效性(这对于脂质体制剂是重要的,因为脂质可能结合/吸附于过滤材料,导致过滤器堵塞,胶体不稳定性和/或整体产品产量的降低)。
③应测定包装前冻干粉末的填充重量和含水量,以评估冻干过程的有效性。
这些过程控制关键点被完整的列在表1中。在脂质体产品生产过程中使用这些过程控制将有助于开发具有良好的批间重现性的高质量产品。
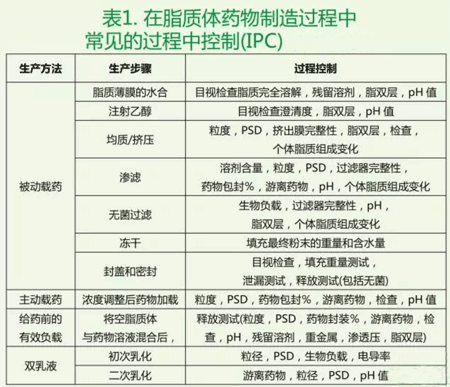
表1 脂质体药物制备过程中常见过程控制
生产过程的不完整流程图/描述以及不完整的工艺参数信息可能反映出一个不全面的控制过程,这可能导致药品质量低下,重现性差。换言之,如果生产过程中的每个步骤没有被很好的界定,而且没有通过过程测试进行仔细的控制,则较终产品可能存在质量控制和批次间变化的问题。在监管方面,如果用于审查的生产过程信息有限,可能增加审查周期时间,较终延迟了批准的时间。
透彻了解生产过程以及使用适当的过程控制,可以实现良好的控制生产过程,并且在生产放大过程中不太可能遇到障碍。通过在产品开发的早期阶段应用设计质量(QbD)原则可以实现对适当过程控制的理解和认知。QBD在开发过程中的应用有助于定义设计空间,为处方和生产过程提供灵活的选择,以实现药品的所需的质量属性。
(4)产品稳定性(7%)
脂质体在热力学上是不稳定的,因此容易存在物理不稳定性,例如在储存期间出现融合或聚集。脂质分子也容易发生化学不稳定性,例如水解(形成溶血脂质)和在储存过程中的氧化降解。稳定性方案中应包括在粒径,脂质降解产物(溶血脂质和脂肪酸含量),相变温度等方面的测试,以确保脂质体产品在储存期间的的物理和化学稳定性。
在制备脂质体产品应用时需要注意的关键方面包括脂质体产品的表征,脂质辅料的CMC /分析方法和验证、生产过程、处方组成和稳定性。这些关键方面可能会影响脂质体产品质量,安全性和有效性,其中粒径和脂质降解产物需要较多的关注。FDA在Doxil®和AmBisome®修订的脂质体指南和生物等效性指导原则中已经明确提出了与粒径数据相关的建议。另外控制脂质降解产物的限制(根据ICH指南)也是不可避免的。
2、非脂质体剂型特异问题
与药物产品相关的质量问题如检测、残留溶剂、重金属、外观、鉴别等则被认为是非特异性的,因为它们也适用于包括片剂、乳剂等的任何制剂类型。例如,没有提供生产溶液与制造设备的相容性研究是属于非特异质量问题的一个例子。
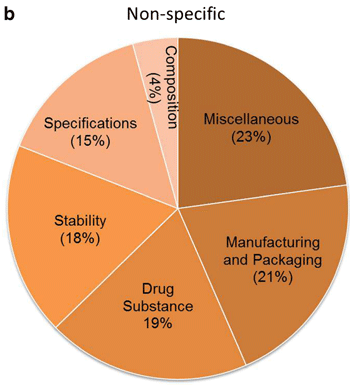
图 非脂质体剂型特异问题统计
除脂质体特异性质量问题外,还有其他问题不是产品特异性的(即与脂质体产品无关)。大多数这些问题被归类为杂项(23%),具体涉及文件不完整(缺少分析证明书、授权书、环境评估/分类排除和cGMP认证)和数据不一致。在提交给审查机构之前,对申请的全面审查可以帮助确保没有数据差异(原始和修订数据,分析证明书和释放规范),并且申请材料包括所有必需的文件。
紧随杂项之后是生产和包装(21%)和原料药(19%)这两个类别。如果产品涉及新化学/分子实体,审评者将着重考虑生产,表征(如外观,鉴定,杂质,测定,残留溶剂等)和稳定性的完整细节。剩余的非特异性问题与药品稳定性(18%),规范(15%)和组成(4%)有关。
其中的几个问题对于药品质量和性能至关重要。例如,在一些申请中,没有进行产品溶液与生产设备的相容性研究,缺少容器封闭性测试,未测试注射用药物的生物负载和颗粒物质。一些申请中缺少使用过程中的稳定性数据。一些脂质体产品在患者给药前需要稀释,因为稀释过程中可能影响产品的物理化学性质,因此要求提供使用过程的稳定性研究。脂质体产品像其他复杂处方产品一样,本质上是复杂的, ICH Q8,Q9和Q10指导原则推荐采用QbD方法。另外在一些申请中,释放和稳定性方面没有测试一些关键质量属性。
苏州微流纳米Vic