制备水溶性药物脂质体的方法常见的有薄膜分散法、注入法、逆向蒸发法和复乳法等,虽然它们操作工序简单,但是在制备过程中,都需要大量使用有机溶剂,难以保证产品的安全性,且不适合进行工业上的大规模生产,因此,在工业生产中没有得到广泛的应用。此外,研究人员发现,脂质体制剂品质的优劣主要取决于其粒度大小及其分布,人体组织器官更倾向于吸收利用粒度小且分布均匀的药物脂质体。
动态高压微射流技术的空穴化作用、剪切力、压力降、冲击力和对射流作用,能使物料颗粒大小骤减,因此,越来越多的人研究将这一技术用于制备纳米脂质体,在这个过程中,有机溶剂用量很少,这点与当今社会的绿色、环保、与环境和谐相处的理念一致,动态高压微射流技术应用于制备脂质体会是今后脂质体研究领域的一大趋势。[1]
本实验采用动态高压微射流技术分别联合逆相蒸发法、薄膜分散法、复乳法和乙醇注入法制备维生素纳米脂质体,以包封率为评价指标,筛选出较好的制备维生素纳米脂质体的方法。
主要试剂及仪器

表1 材料与试剂

表2 仪器设备
实验方法:
本实验采用四种经典、传统、适用于水溶性药物的脂质体制备方法薄膜分散法、逆相蒸发法、复乳法和乙醇注入法,分别联合动态高压微射流技术(依次命名为薄膜分散一微射流高压均质法、逆相蒸发一微射流高压均质法、复乳一微射流高压均质法、乙醇注入一微射流高压均质法)来制备维生素C纳米脂质体。
1)薄膜分散一微射流高压均质法
称取配方量的卵磷脂、胆固醇与适量无水乙醇混合后,置于250mL圆底烧瓶中减压蒸发去除乙醇,使烧瓶壁上形成一层均匀的薄膜。然后加入一定量的维生素C双蒸水溶液,旋转洗膜15min左右,得到脂质体悬液较后将悬液水浴声一段时间即制得较均匀的乳白色维生素C脂质体悬浮液。
将上述制得的脂质体悬液在120MPa下,用微射流高压均质机处理两次,即得维生素纳米脂质体。
2)逆相蒸发一微射流高压均质法
称取配方量的卵磷脂、胆固醇与适量无水乙醇混合形成油相,然后和一定量的维生素C双蒸水溶液于250mL圆底烧瓶充分混合,再减压蒸发去除乙醇,得到脂质体悬液较后将悬液水浴声一段时间即制得较均匀的乳白色维生素C脂质体悬浮液。
将上述制得的脂质体悬液在120MPa下,用微射流高压均质机处理两次,即得维生素C纳米脂质体。
3)复乳一微射流高压均质法
称取配方量的卵磷脂、胆固醇与适量无水乙醇混合形成油相,然后加入一小部分维生素C双蒸水溶液,置于250mL圆底烧瓶中充分混合,再减压蒸发去除部分乙醇,然后加入剩余的维生素C双蒸水溶液再继续减压蒸发去除剩余乙醇,即得脂质体悬液较后将悬液水浴声一段时间即制得较均匀的乳白色维生素C脂质体悬浮液。
将上述制得的脂质体悬液在120MPa下,用微射流高压均质机处理两次,即得维生素C纳米脂质体。
4)乙醇注入一微射流高压均质法
称取配方量的卵磷脂、胆固醇与适量无水乙醇混合形成油相,该溶液经注射器缓慢注射到磁力搅拌下的维生素C双蒸水溶液中,去除乙醇后即得脂质体悬液较后将悬液水浴声一段时间即制得较均匀的乳白色维生素C脂质体悬浮液。
将上述制得的脂质体悬液在120MPa下,用微射流高压均质机处理两次,即得维生素C纳米脂质体。
实验结果
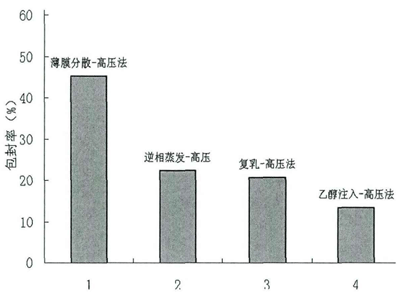
图1 微射流高压均质联合制备方法对维生素C纳米脂质体包封率的影响
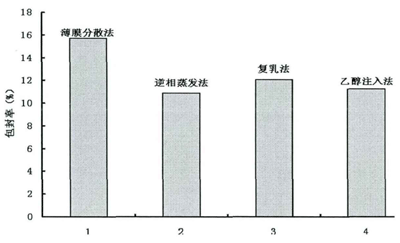
图2 传统制各方法对维生素C脂质体包封率的影响
由图1与图2可知,各种传统脂质体制备方法联用微射流高压均质后制备的脂质体,其包封率大小相差甚远,以薄膜分散一高压均质法制得的脂质体包封率大至,乙醇注入-高压法制得的脂质体包封率小至,其他两种方法相差不大,这说明薄膜分散法和高压具有良好的协同性,因此本实验选用薄膜分散一高压法制备维生素C纳米脂质体。
制备压力大小对维生素纳米脂质体包封率的影响
选择同一处方,固定其他组分的比例不变,即制备温度50℃,保持VC浓度为5mg/ml,卵磷脂:胆固醇=4:1,卵磷脂:无水乙醇=1:10, Tween-80:总脂材=3:10,VC:总脂材=1:10,压力处理次数2次,考察处理压力大小(80MPa、100MPa、120MPa、140MPa、160MPa)对维生素C纳米脂质体包封率的影响,测定包封率,结果如下图
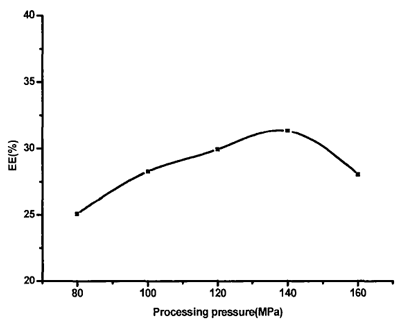
图3 处理压力大小对维生素C纳米脂质体包封率的影响
从图3可以看出,压力小于140MPa时,随着压力的增大,包封率也逐渐增大。当压力为140MPa时,包封率大至;但当压力大于140MPa时,随着压力的增大,包封率反而减小,其原因可能是适当的压力能促进磷脂分子自由组装形成脂质体,但是压力过大,则会迫使脂质体内包封的维生素C渗漏出来,从而使包封率减小。因此,本实验采用制备压力为140MPa。
苏州微流纳米Vic